Uge 37 - 2021
Testning for RS-virus er normalt kun indiceret i de tilfælde, hvor barnet er så påvirket, at det skal indlægges
Ny vaccine mod helvedesild
Testning for RS-virus er normalt kun indiceret i de tilfælde, hvor barnet er så påvirket, at det skal indlægges
Som tidligere rapporteret i EPI-NYT 27/21 og 35/21, har vi i Danmark siden juni oplevet en ekstraordinær forekomst af RS-virus. Særligt i de seneste uger er smittetallene steget epidemisk til et niveau, der ligger 3-4 gange over det normale for RS-sæsonen, figur 1. Usædvanligt høje RS-virus smittetal er også set i andre lande, bl.a. i Norge, Japan, Australien og New Zealand.
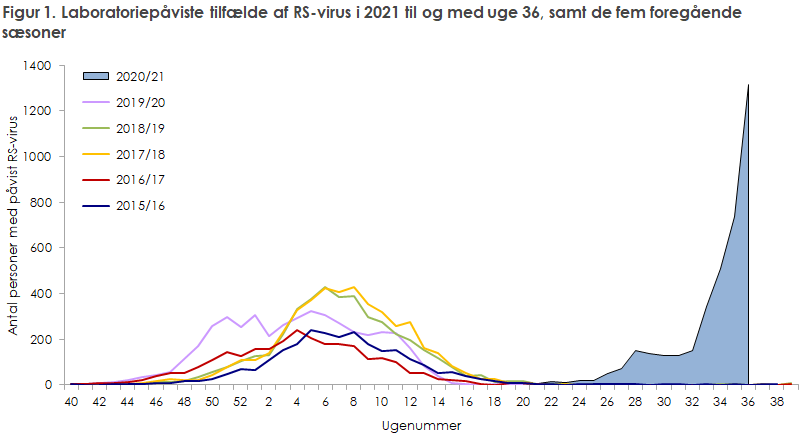
Yderligere grafer og tabeller med de seneste RS-virus-smittetal ses her.
Personer i alle aldersgrupper kan smittes med RS-Virus. Særligt de mindste børn kan udvikle alvorlig sygdom med behov for understøttende behandling, herunder respiratorisk støtte. Mens ældre børn og voksne typisk kun får milde luftvejssymptomer.
De mange smittede børn med RS-virus skaber aktuelt et stort pres hos landets praktiserende læger, vagtlæger, akutmodtagelser og børneafdelinger.
Statens Serum Institut og Dansk Pædiatrisk Selskab ønsker her at præcisere indikationerne for testning af børn for RS-virus:
- Testning for RS-virus hos tidligere raske børn er normalt kun indiceret i de tilfælde, hvor barnet er så påvirket, at det skal indlægges. Test kan da medvirke til at afklare behandlingsbehov og ikke mindst behov for isolation.
- Hos børn med let til moderat luftvejssygdom, der ikke er indlæggelseskrævende, er det ikke indiceret med rutinemæssig test for RS-virus.
(A.S. Gjerløv, M.-L. von Linstow, N. Fisker, Dansk Pædiatrisk Selskab, R. Trebbien, Virus og Mikrobiologisk Specialdiagnostik, L.S. Vestergaard, Afdeling for Infektionsepidemiologi og Forebyggelse)
Ny vaccine mod helvedesild
En ny vaccine mod helvedesild (herpes zoster) bliver tilgængelig i Danmark fra den 1. oktober 2021. Vaccinen, Shingrix, fik allerede markedsføringstilladelse i EU i 2018, men kan først bestilles i Danmark nu.
Vaccinen er godkendt til voksne fra 50 år eller ældre til beskyttelse mod herpes zoster og langvarige nervesmerter efter herpes zoster (postherpetisk neuralgi). Desuden kan vaccinen anvendes til voksne fra 18 år eller ældre, som pga. kompromitteret immunsystem har forhøjet risiko for herpes zoster.
Shingrix er en rekombinant, adjuveret vaccine og indeholder et protein fra varicella zoster-virus, som er det virus, der forårsager skoldkopper og herpes zoster. Shingrix er en inaktiveret vaccine og indeholder derfor ikke levende svækket varicella zoster-virus i modsætning til vaccinen Zostavax, der også er godkendt til beskyttelse mod helvedesild.
Dosering
Det primære vaccinationsprogram består af to doser med et anbefalet interval på to måneder. Man anbefaler, at begge doser gives indenfor seks måneder, men selv om denne tid overskrides, startes der ikke forfra. For personer som er, eller som forventes at blive immunkompromitterede, og som derfor kan have gavn af at blive beskyttet hurtigere mod herpes zoster, kan man administrere anden dosis helt ned til én måned efter første dosis.
Vaccinen administreres intramuskulært.
Der er endnu ikke klarlagt behov for revaccination efter det primære vaccinationsprogram.
Shingrix kan gives til personer, der tidligere er vaccineret med levende svækket skoldkoppevaccine. Shingrix er ikke indiceret til forebyggelse af primær varicella-infektion (skoldkopper).
Fase III-studier har vist, at Shingrix kan gives samtidig med inaktiverede influenzavacciner, Pneumovax (PPV 23) og diTe-booster/diTeki-booster, uden dette påvirker immunresponset. På Statens Serum Instituts (SSI) hjemmeside kan du læse mere om vejledende intervaller mellem vaccinationer med levende og inaktiverede vacciner.
Vaccineeffektivitet
Beskyttelsen mod helvedesild efter vaccination med Shingrix er undersøgt i to fase III-studier. I det ene studie reducerede vaccination med Shingrix forekomsten af herpes zoster og postherpetisk neuralgi betydeligt hos patienter i alderen 50 år og derover. I studiet fik 7.695 personer Shingrix og 7.710 personer placebo. Efter en opfølgningstid på gennemsnitlig tre år havde seks voksne i Shingrix-gruppen haft herpes zoster sammenholdt med 210 voksne i placebogruppen. Efter fire års opfølgningstid havde ingen i Shingrix-gruppen fået postherpetisk neuralgi sammenholdt med 18 tilfælde i placebogruppen. Således blev der vist en vaccineeffektivitet på 97% i beskyttelsen mod helvedesild og 100% beskyttelse mod postherpetisk neuralgi for voksne over 50 år.
I det andet studie undersøgte man specifikt virkningen hos voksne over 70 år. Sammenholdt med resultaterne for de +70-årige deltagere i førstnævnte studie viste Shingrix en vaccineeffektivitet på 91% mod herpes zoster og 89% mod postherpetisk neuralgi blandt gruppen af +70-årige.
De to ovennævnte studier inkluderede ikke personer med tidligere tilfælde af herpes zoster.
Effekten af Shingrix er også undersøgt hos voksne på 18 år og derover med forhøjet risiko for at udvikle herpes zoster. I et studie med personer, som havde fået autolog stamcelletransplantation, var effekten mod herpes zoster 68%. I et andet studie med personer, som havde maligne hæmatologiske sygdomme, var effekten 87%.
Bivirkninger
Sikkerheden af Shingrix er vurderet ved kliniske studier med flere end 15.000 voksne. Bivirkninger rapporteret efter markedsføring er også medtaget i sikkerhedsprofilen.
De hyppigst rapporterede bivirkninger for voksne over 50 år, samt voksne over 18 år med forhøjet risiko for herpes zoster, var smerter omkring injektionsstedet (68,1%), muskelsmerter (32,9%), træthed (32,2%) og hovedpine (26,3%). Desuden var hyppigheden af bivirkninger i form af gastrointestinale symptomer såsom kvalme, opkastning, diarré og/eller abdominale smerter over 10%. Medianvarigheden af bivirkningerne var 2-3 dage. Sikkerhedsprofilen for de voksne immunkompromitterede ≥18 år var konsistent med den, der blev observeret hos de +50-årige.
For de øvrige bivirkninger samt kontraindikationer og forhold omkring fertilitet, graviditet og amning, henvises til produktresumeet.
Opbevaring
Shingrix skal opbevares mellem 2 °C og 8 °C, og al håndtering uden for køleskab skal minimeres. Vaccinen må aldrig fryses eller opbevares over 30 °C.
Administration
Shingrix skal rekonstitueres før administration. Pulveret og væsken blandes, hvorefter det rystes forsigtigt, indtil pulveret er fuldstændigt opløst. Den rekonstituerede vaccine er en opaliserende, farveløs til lys brunlig væske. Efter rekonstitution skal vaccinen anvendes straks eller opbevares i køleskab og administreres indenfor seks timer.
Bestilling
Shingrix kan bestilles fra den 1. oktober på elektronisk blanket 6 under SSI varenr. 104035.
(C.H. Espensen, N.U. Friis, Afdeling for Infektionsepidemiologi og Forebyggelse)